皆さん、こんにちは。草原の探究者、キツネ博士じゃ。 わしらの体を作っておる細胞たちは、無限に分裂できるわけではない。ある回数、分裂すると、ピタッと増えるのをやめてしまう。これは「ヘイフリック限界」と呼ばれ、いわば細胞自身の寿命のようなものじゃな。この「分裂停止(細胞老化)」は、体の老化や様々な病気と深く関わると考えられておるが、その詳しい仕組みにはまだ謎が多いんじゃ。
そこで今回紹介する研究(Chan et al., eLife, 2022)は、この細胞老化の謎に、現代科学の粋を集めた最新技術で挑んだ、非常に野心的なものじゃよ。まるで細胞の中を隅々までスキャンするように、その変化を徹底的に追跡したんじゃ。
細胞老化を丸裸に!最新技術の総動員
研究チームは、ヘイフリック博士が最初に細胞老化を発見した時と同じ「WI-38」というヒトの肺の線維芽細胞を使って、細胞が若々しく分裂している状態から、分裂を停止する老化状態に至るまでの全過程を、時間を追って観察した。
使われたのは、まさに現代科学の「七つ道具」じゃ!
- 遺伝子の設計図(RNA-seq, scRNA-seq): どんな遺伝子が働いているか
- 細胞の働き手(プロテオミクス): どんなタンパク質が作られているか
- エネルギーや材料(メタボロミクス): どんな代謝物質があるか
- 設計図の開き具合(ATAC-seq): 遺伝子(DNA)のどの部分がアクセス可能か
これらを組み合わせることで、細胞老化という現象を、かつてない解像度で多角的に捉えようとしたんじゃ。
老化は突然やってこない?徐々に変化する細胞の姿
まずわかったのは、細胞老化は、ある日突然スイッチが入るようなものではない、ということじゃ。シングルセルRNA-seq(細胞一個一個の遺伝子発現を調べる技術)で詳しく見ると、老化に関連する遺伝子の変化は、細胞がまだ元気に分裂している早い段階から、少しずつ始まっておったんじゃ。まるで、木々の葉が秋に一斉に色づくのではなく、少しずつ緑から黄色、そして赤へとグラデーションを描くように変化していくようじゃな。
驚きの変身!老いた細胞は「修理屋」になっていた!?
そして、ここからが今回の研究の最も驚くべき発見じゃ。 様々なデータを統合して分析した結果、分裂を停止した老化細胞は、単に衰えただけでなく、全く別の種類の細胞に姿を変えようとしていることがわかったんじゃ!
その姿とは、「筋線維芽細胞(ミオフィブロブラスト)」。これは、傷ついた組織を修復するために現れる、いわば「専門の修理屋細胞」じゃ。普段はおとなしい線維芽細胞が、傷などの刺激を受けると、この修理屋に変身することが知られておる。
老化細胞の遺伝子やタンパク質を調べると、この筋線維芽細胞の特徴(例えば、α平滑筋アクチン(ACTA2)というタンパク質や、コラーゲンの産生に関わる遺伝子群)が、非常によく似ておったんじゃ。これは、「上皮間葉転換(EMT)」に似たプロセス、線維芽細胞の場合で言えば「線維芽細胞-筋線維芽細胞転換(FMT)」が、細胞老化の過程で自然に起こっている可能性を示唆しておる。
FMT(線維芽細胞-筋線維芽細胞転換)とは何か?
FMTとは、Fibroblast to Myofibroblast Transition の略で、日本語では「線維芽細胞から筋線維芽細胞への転換」という意味じゃ。
もともと、線維芽細胞というのは、わしらの体の組織の中で、コラーゲンなどの細胞外マトリックス(組織の足場となる物質)を作ったり、組織の構造を維持したりする、いわば「普通の建築作業員」のような細胞じゃ 。
ところが、組織が傷ついたり、強いストレスを受けたりすると、この線維芽細胞は「筋線維芽細胞」という、よりパワフルな細胞に変身(転換)することがあるんじゃ 。これがFMTじゃな。
変身のスイッチは?YAP/TEAD1とTGF-β2
では、何がこの「変身」のスイッチを押しておるのじゃろうか? 研究チームは、遺伝子の働きを調節する「司令塔」役のタンパク質にも注目した。ATAC-seq(DNAの開き具合を調べる技術)で、老化に伴ってアクセス可能になるDNA領域を調べ、そこに結合する司令塔を予測したんじゃ。
すると、「YAP1/TEAD1」という転写因子複合体と、「TGF-β2」というシグナル伝達物質が、この変身劇の重要な容疑者として浮かび上がってきた。これらは、細胞の増殖や分化、そしてまさにEMTやFMTを制御することが知られておる司令塔たちじゃ。
実際に、YAP1/TEAD1の働きを阻害する薬剤(ベルテポルフィン)を老化した細胞に投与すると、筋線維芽細胞のような特徴を示す遺伝子の多くが、元の状態に戻ることも確認された。これは、YAP1/TEAD1が細胞老化に伴う「変身」に、直接関与している強い証拠じゃな。
舞台裏では何が?代謝とエピゲノムの変化
さらに研究は、この変身劇の舞台裏で起きている変化にも光を当てた。 メタボローム解析からは、老化細胞では脂肪酸をエネルギー源として利用する経路が活発になる一方で、糖を別の物質(グリコサミノグリカンなど)に作り変える経路も活性化していることがわかった。これは、修理屋として働くために必要なエネルギー産生と、細胞外マトリックス(組織の足場)を作るための材料生産が、同時に行われていることを示唆しておる。
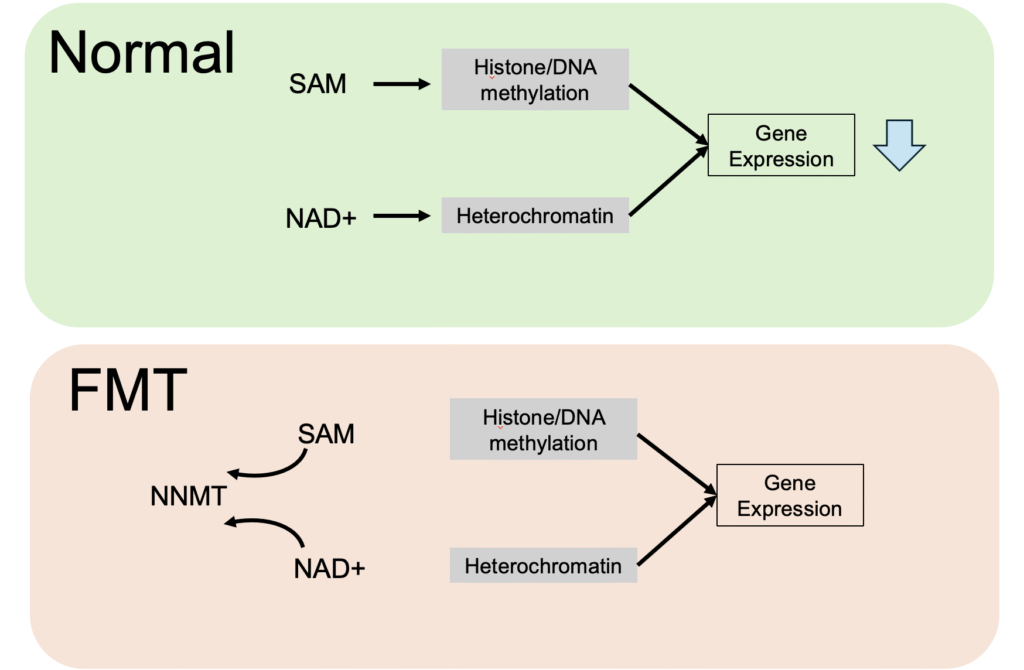
また、興味深いことに、NNMTという酵素が老化の早い段階から増加していた。この酵素は、遺伝子のスイッチをOFFにする「メチル化」に必要な材料(SAM)と、細胞のエネルギー通貨に関わるNAD+の両方を消費してしまう。これが、老化に伴ってDNAの通常閉じている領域(NADs/LADsと呼ばれるヘテロクロマチン領域)が開きやすくなる(ATAC-seqで観察された)ことに関与しているのかもしれん。まるで、普段は鍵のかかっている部屋の扉が、少しずつ開いていくような変化じゃな。
結論:細胞老化の新たな理解と未来への展望
今回の多角的な研究は、細胞老化(ヘイフリック限界)に対する我々の理解を大きく塗り替えるものじゃった。
- 細胞老化は、単なる停止ではなく、筋線維芽細胞への「変身(FMT様プロセス)」を伴う、能動的な状態変化であること。
- この変身は、YAP1/TEAD1やTGF-β2といったシグナルによって制御されている可能性があること。
- この過程には、代謝の大規模な再編と、NNMTの活性化を介したエピゲノム(DNAの開き具合)の変化が関与していること。
この「老化=FMT」という新しい視点は、なぜ老化細胞が組織の線維化(組織が硬くなる病気)や炎症に関わるのか、新たな説明を与えるかもしれん。そして、YAP1/TEAD1のような変身のスイッチを制御することが、老化に関連する病気の新しい治療法に繋がる可能性も秘めておる。
細胞がたどる運命の複雑さと巧妙さには、まだまだ驚かされることばかりじゃな。
それでは、また次の記事で会おう。キツネ博士じゃった。
【今回ご紹介した研究】
- 論文タイトル: Novel insights from a multiomics dissection of the Hayflick limit
- 著者: Chan, M., et al.
- 発表年: 2022
- 掲載誌: eLife, 11, e70283
- DOI: https://doi.org/10.7554/eLife.70283



コメント